Il Blog di Andrea Deledda, Biologo nutrizionista http://www.nutrizionecagliari.it/
Cerca nel blog
giovedì 21 novembre 2024
Ictus: come i nutrienti possono aiutarci prima (e dopo)
sabato 6 luglio 2024
I nostri piccoli eroi: i mitocondri
Il mitocondrio è l'organello che fornisce la maggior parte dell'energia cellulare, sfruttando l'energia chimica dei legami presenti nelle sostanze nutritive.
Alla fine del 19° secolo Benda notò delle strutture intracellulari simili ai batteri, che funzionavano come organismi elementari; chiamò queste strutture “mitocondri”, formando la parola dalle parole greche “mitos” (filo) e “chondros” (granuli).
 |
| https://it.pinterest.com/pin/599189925414126768/ |
domenica 29 ottobre 2023
Aminoacidi essenziali: perché li consiglio
In pratica il maggior aumento delle concentrazioni plasmatiche di aminoacidi che si ha con l'integrazione di EAA favorisce maggiore aumento di muscolo rispetto a cibo e altri integratori perché entrano più facilmente nel muscolo dove permettono l'effetto anabolico.
Gli EAA sono particolarmente indicati nei periodi di deficit calorico in cui si punta a ridurre la massa grassa, perché salvaguardano dalla perdita di muscolo.
La stimolazione dell'anabolismo muscolare avviene anche in persone che non praticano movimento, sono per questo ottimi in pazienti immobilizzati e anziani, mentre per dimostrare questo nei giovani servono più studi.
Gli EAA possono essere assunti prima, durante e dopo l'attività fisica, per massimizzare il loro effetto anabolico.
Altre condizioni che possono beneficiare dell'uso sono: sarcopenia, infezioni acquisite durante cure a lungo termine, ridotta funzionalità fisica e insufficienza cardiaca. "Gli effetti benefici degli EAA sono stati segnalati anche nelle seguenti condizioni o situazioni: riabilitazione; ictus; riposo a letto/immobilizzazione; malattia delle arterie periferiche; insufficienza renale; infiammazione; malattia critica; cancro ai polmoni; fibrosi cistica; malattia polmonare cronica ostruttiva; guarigione delle ferite; lesione cerebrale; sindrome metabolica e fattori di rischio cardiovascolare; obesità; grasso nel fegato e diabete. È importante sottolineare che in tutti questi studi sono stati osservati effetti benefici nonostante l'assenza di controllo sul consumo degli EAA contenuti nelle proteine alimentari, suggerendo l'importanza dell'assorbimento rapido e completo degli EAA liberi in circostanze cliniche in cui la digestione può essere compromessa e la resistenza anabolica è prevalente".
Sottolineo che si tratta di malattie che hanno in comune un'alterazione della funzione mitocondriale, che beneficia della supplementazione di EAA.
Questi supplementi hanno un costo superiore a parità di peso rispetto alle altre fonti proteiche, ma una maggiore convenienza in rapporto all'effetto.
Chiedete comunque sempre consiglio al professionista prima di assumerli (sicuramente controindicati in caso di assunzione di psicofarmaci e di fenilchetonuria).
Aggiornamento 12/7/2024
L'incremento di muscolatura negli anziani stimolato da 3,6g di aminoacidi essenziali è molto maggiore di quello di 15g di proteine whey. Questo è probabilmente dovuto alla miglior efficienza nell'assorbimento intestinale.
lunedì 12 luglio 2021
HMO: perché i bambini allattati stanno bene
Gli HMO sono zuccheri non digeribili presenti nel latte materno, che hanno il compito principale di nutrire il microbiota del neonato.
 |
| https://thriftyniftymommy.com/breastfeeding-memes/ |
Oggi si possono utilizzare come supplementi, con tutti i vantaggi del caso. Ad esempio promuovere la crescita di specie benefiche, come i bifidobatteri (in particolare B. infantis), ma anche Firmicutes, Actinobacteria, Bacteroides e Lachnospiraceae. Parallelamente si riducono i batteri cattivi come Enterococcus, Proteobacteria, Streptococcus, Rothia, Enterococcus e Clostridia.
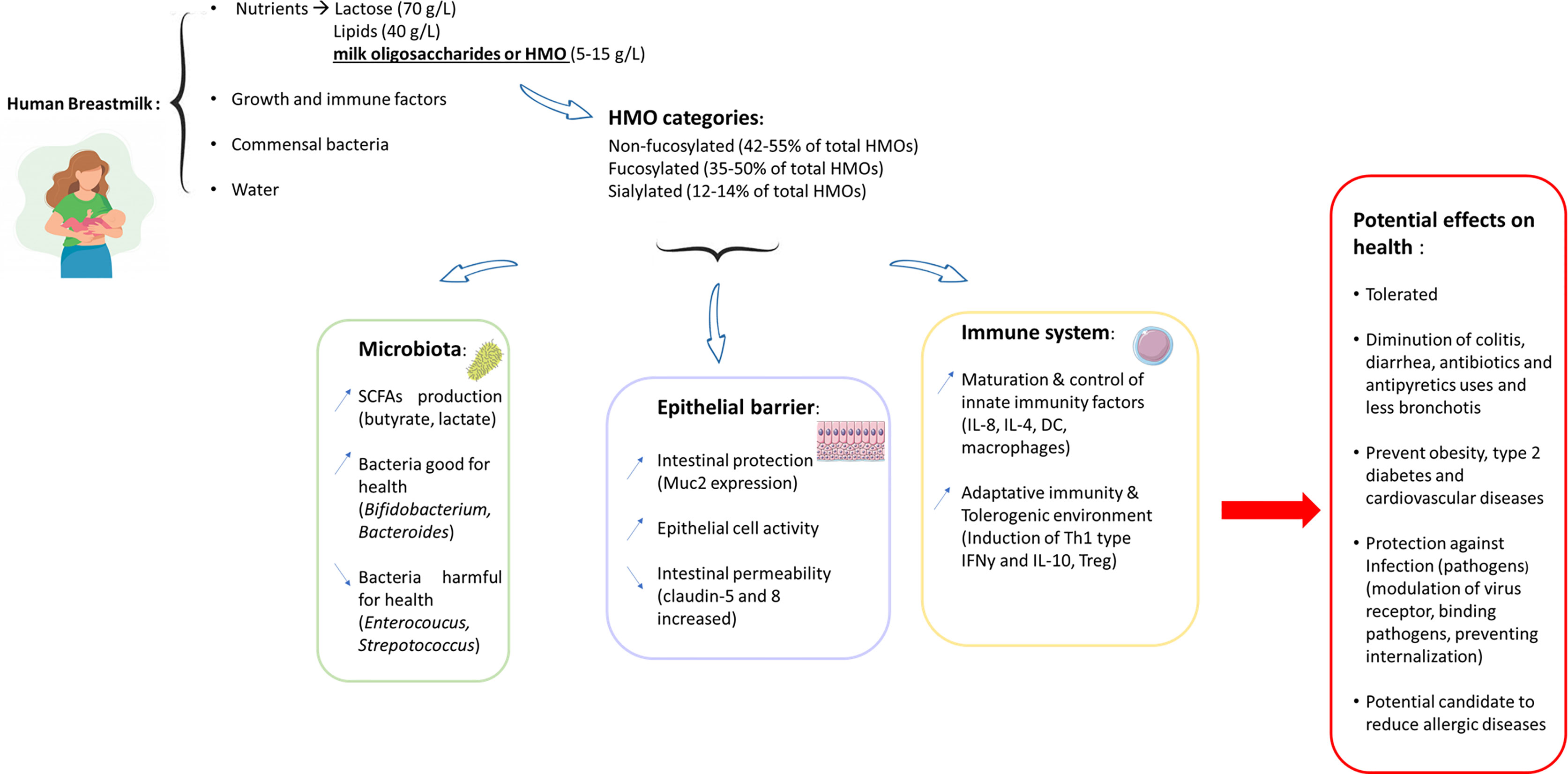 |
| clicca sull'immagine per ingrandire |
Infatti solo l'allattamento fornisce batteri buoni (B. breve e B. infantis) e zuccheri specifici (HMO) in quantità sufficienti e che proteggono dall'infiammazione, dalla permeabilità intestinale e dalle infezioni che causano enterocolite necrotizzante, la principale causa di morte nei prematuri.
"La peristalsi (ridotta motilità intestinale), la cattiva digestione delle fonti di nutrienti e una barriera intestinale compromessa possono rendere la mucosa suscettibile all'invasione di agenti patogeni opportunisti nell'ambiente intestinale. Il conseguente squilibrio tra danno e riparazione delle cellule epiteliali porta a un circolo vizioso di cattiva digestione, invasione batterica, attivazione immunitaria e infiammazione incontrollata"
Viceversa uno svezzamento precoce favorisce un cambio accelerato del microbiota (colonizzazione precoce di Ruminococcus gnavus) che non risulta protettivo dall'asma e ne aumenta il rischio.